Tirzepatide減肥適應症獲FDA批准,禮來市值逼近6000億美元
11月8日,禮來宣布Zepbound(Tirzepatide)獲FDA批准用於慢性體重管理,適用於肥胖(BMI≥30kg/m2)或超重(BMI≥27kg/m2)成人患者,且這類患者伴有與體重相關合並症,如高血壓、血脂異常、2型糖尿病、阻塞性睡眠呼吸暫停或心血管疾病。

消息公布後,禮來股價上漲3.2%,市值達到5877.45億美元,逼近6000億美元大關。
Tirzepatide是一款每周注射1次的GLP-1R/GIPR雙重激動劑,於2022年5月首次獲FDA批准上市,用於治療2型糖尿病。
FDA此次批准主要是基於SURMOUNT-1和SURMOUNT-2研究的積極數據。
針對肥胖的非2型糖尿病患者的SURMOUNT-1研究結果顯示,Tirzepatide達到了兩個共同主要終點:與安慰劑相比,Tirzepatide組患者體重較基线變化百分比更高,並且Tirzepatide組患者達到體重減輕至少5%的比例更高。
與安慰劑(2.4%,2kg)相比,接受5mg Tirzepatide的受試者體重平均減輕了16.0%,10mg組平均減輕了21.4%,而15mg組平均減輕了22.5%(相當於24kg)。此外,Tirzepatide組分別有89%(5mg)和96%(10mg和15mg)的患者體重減輕了至少5%,而安慰劑組僅有28%患者體重減輕5%。
針對肥胖或超重伴2型糖尿病患者的SURMOUNT-2研究結果顯示,與安慰劑相比,Tirzepatide(10mg和15mg)在治療72周時取得了優於安慰劑的減肥效果。與安慰
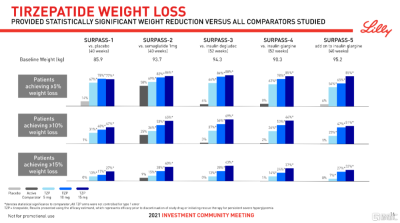
劑相比,該研究同時滿足共同主要終點和所有關鍵次要終點。
與安慰劑(3.3%、3.2kg)相比,10mg組患者體重平均減輕了13.4%(13.5kg),15mg組平均體重減輕了15.7%(15.6kg)。此外,10mg、15mg組分別有81.6%和86.4%的患者減重5%以上,而安慰劑組比例爲30.5%,達到了共同主要終點。
Tirzepatide還達到了所有關鍵的次要終點,包括降低A1C和其他心髒代謝參數。與安慰劑相比,A1C降幅與成人2型糖尿病患者的SURPASS試驗相似。
此外,禮來也在中國遞交了Tirzepatide的減肥適應症上市申請,目前正在審評中。
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:Tirzepatide減肥適應症獲FDA批准,禮來市值逼近6000億美元
地址:https://www.twnewsletter.com/article/21859.html
